OpenText Documentum Content Management for Life Sciences
ライフサイエンス分野におけるGxP準拠のコンテンツ管理を徹底
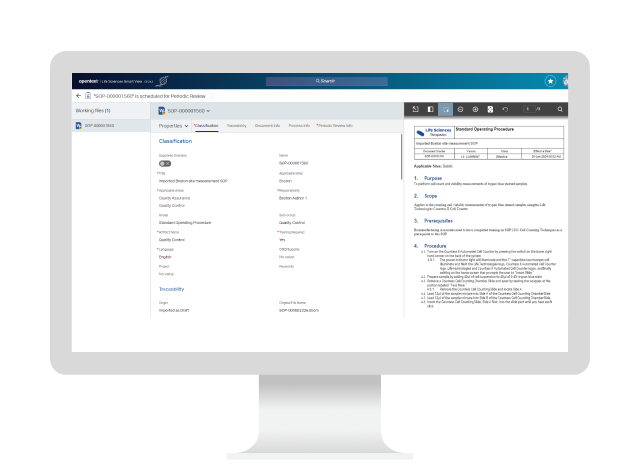
ライフサイエンス分野のコンテンツは次の規制当局の検査に対応できていますか?
文書、サイロ化されたシステムとプロセス、規制のハードルに溺れているのは、あなただけではありません。コンテンツを管理するには、現代のライフサイエンスのペースに合わせて、より速く、よりスマートに構築された、より良い方法があります。
OpenText Documentum CM for Life Sciencesを選ぶ理由
OpenTextだけが、25年以上にわたるライフサイエンスの専門知識と、グローバルリーダーから信頼されている実証済みのプラットフォームを組み合わせています。当社のソリューションはコンプライアンスを超え、イノベーションを促進し、迅速化を可能にし、自信を持ってクラウドでの拡張を実現します。
- 25年以上
業界で実証済み、GxP対応
21 CFR Part 11、監査証跡、電子署名、規制基準のサポートが組み込まれた、ライフサイエンス向けに設計されたソリューションをご利用ください。 - 3.5x
毎月追加処理される文書の数
デジタルワークフローを活用して、時間を節約し、リスクを軽減し、真のビジネス成長のための余地を作りましょう。
お客様事例を読む - 3
ライフサイエンス専用のソリューション
臨床、規制、品質に関する文書を1つのシステムで安全に処理することで、科学と同じ速さでコンテンツを移動させることができます。
ユースケース
臨床試験から商業販売に至るまで、チームはOpenText Documentum CM for Life Sciencesを活用して、規制されたコンテンツを迅速かつ正確に管理し、コンプライアンスを簡素化し、生産性を向上させ、救命治療をより早く市場に投入しています。
-
タクソノミー、ライフサイクル、ワークフローを使用して、ICH準拠の申請を自動化します。メタデータ駆動型アクセス制御を通じて、OpenText Documentum CM for Regulatoryで編集、マージ、安全なアーカイブを有効にします。
製品概要を読む -
-
OpenText Documentum CM for Quality and Manufacturingの強力で管理されたテンプレートを使用し、安全で追跡可能な印刷と追跡を含む、GMP準拠のドキュメントの一貫した品質、構成、管理をサポートします。
製品概要を読む -
CTMS、LIMS、LMS、QMS、ERPなどのツールにリンクすることで、よりスマートに作業できます。そうすることで、情報が常に接続され、管理が容易になります。
-
チームがラボにいても自宅にいても、ドキュメントを安全に共有および編集し、作業を保護しながら正しい方向に進めることができます。
-
ライフサイエンスチーム向けに設計された構築済みのソリューションを使用して、IDMPやeTMFなどの重要な業界ルールを迅速に設定し、遵守することができます。
主な機能
ライフサイエンスのすべての文書管理を1つの簡単なシステムに統合します。臨床試験から品質、製造、薬事業務まで、整理整頓、ルール遵守、スマートな業務に必要なツールを入手できます。

GxPコンプライアンスフレームワーク
監査証跡、電子署名、自動化された制御を用いた検証サポートを提供し、規制遵守を確保し、検査リスクを軽減します。

統合リポジトリ
臨床、規制、製造のファイルをまとめて安全に保管し、すべてを一か所で簡単に見つけて管理できるようにします。

クラウドまたはオンサイト導入
DockerやKubernetesなどのスマート技術を活用し、オンプレミスまたはクラウドでお好みの方法で展開し、更新やスケーリングを簡単に行えます。

すぐに使えるワークフロー
業界向けに構築されたワークフロー、テンプレート、フォルダにより、迅速に作業を開始し、グローバル基準に準拠することができます。

自動化された文書チェック
不足書類や間違った書類を有用な図表やレポートで発見し、問題になる前に迅速に修正します。

アプリの統合
システムを既存の品質、トレーニング、公開アプリにリンクし、プログラムを切り替える必要がないようにします。
スマートタグ付けと文書追跡
組み込みのルールとメタデータタグを使用して、最初から最後まで文書を簡単かつ一貫して適切に管理します。
ご購入
ライフサイエンス組織のニーズを満たすように設計されたOpenText Documentum CM for Life Sciencesの拡張可能で将来を見据えた3つのプラン(eTMF、Quality and Manufacturing、Regulatory)をご覧ください。
| スワイプして詳細を見る | チームの生産性を向上 | 機能横断的な卓越性を構築 | 境界を越えた架け橋 |
|---|---|---|---|
長期的なデータコンプライアンスとIT運用を簡素化し、クラウドへの移行を加速させます。
| チームの生産性を向上 | 機能横断的な卓越性を構築 | 境界を越えた架け橋 | |
|---|---|---|---|
アドオン | |||
業界および部門別のソリューションにより、コンテンツサービスプラットフォームを強化します。
| チームの生産性を向上 | 機能横断的な卓越性を構築 | 境界を越えた架け橋 | |
|---|---|---|---|
アドオン | |||
アドオン | |||
アドオン | |||
アドオン | |||
アドオン | |||
AIを活用したコンテンツ管理ソリューションで、組織の知識を理解して行動に移します。
| チームの生産性を向上 | 機能横断的な卓越性を構築 | 境界を越えた架け橋 | |
|---|---|---|---|
アドオン | |||
アドオン | |||
統合
これらの統合機能を使って、ライフサイエンス分野のコンテンツをつなげましょう。
生命科学分野におけるOpenText Documentumコンテンツ管理の価値を加速
Add-ons
強力な拡張機能を使用して、ライフサイエンス向けのOpenText Documentum CMへの投資を最大限に活用してください。
-
AIを活用したコンテンツアシスタントを使用して、ビジネスコンテンツをより迅速に見つけ、手作業を排除
セキュアなAIコンテンツアシスタントで、生産性の新たな高みを目指す
-
効率的なアプリケーションデコミッションでクラウド移行を簡素化
拡張性があり、経済的でコンプライアンスに準拠したアーカイブソリューションを使用して、ITコストを削減し、最新のクラウドベースのアーキテクチャへの移行を加速させます。
-
どのようなリポジトリやフォーマットにも対応するナレッジディスカバリで洞察を得る
AIと機械学習を使用して、非構造化データを簡単に見つけて理解
-
紙やデジタルコンテンツを実用的なインサイトに変換
AIと機械学習を活用してコンテンツプロセスを自動化し、情報を適切なユーザーとシステムに安全にルーティングし、必要なときに必要な場所で正確な情報を入手できるように
統合
日常的に使用するシステムをエンタープライズコンテンツ管理ツールと統合します。
-
ビジネス・プロセスにコンテンツとコラボレーションを組み込むことで効率化を促進します
SAP® Solutions
-
Microsoft 365を進化させ、よりスマートな情報管理を実現
Microsoft 365™
-
Salesforceでコラボレーションを強化し、プロセスを自動化し、効率を最大化します
Salesforce®
導入
OpenTextは、ライフサイエンス向けのOpenText Documentum Content Management for Life Sciencesに対して柔軟な導入オプションを提供しています。
-
あなたのクラウド、あなたのコントロール
OpenText Private Cloud
-
OpenText Thrust APIを使用してAIに備える
OpenText Developer CloudからのAPI
-
リソースを解放し、パフォーマンスを最適化し、問題に迅速に対処
OpenText Off Cloud Managed Services
プロフェッショナルサービス
OpenTextのプロフェッショナルサービスは、エンドツーエンドのソリューション導入と包括的なテクノロジーサービスを組み合わせて、システムの改善を支援します。
-
情報管理に詳しい信頼できるパートナーを探す
成功への道のり
-
情報管理を加速させる
コンサルティングサービス
-
最新のソリューションでビジネスを未来へ推進
次世代のサービス
-
情報管理ソリューションの可能性を最大限に引き出す
カスタマーサクセスサービス
パートナー
OpenTextは、お客様が適切なソリューションやサポート、そして期待通りの結果を得られるよう支援します。
-
OpenTextのパートナーディレクトリを検索
パートナーを探す
-
OpenTextのパートナーソリューションカタログを見る
アプリケーションマーケットプレイス
-
OpenTextの製品とソリューションを強化する、業界をリードする組織
戦略的パートナー
トレーニング
OpenTextのラーニングサービス は、知識とスキルを加速させるための包括的なイネーブルメントと学習プログラムを提供します。
-
OpenText Documentum Content Management for Life Sciencesラーニングパス
このコースでは、OpenText Documentum CM for Quality and Manufacturing ソリューションの包括的な機能概要を提供します。ワークフロー、ライフサイクル、監査、検索機能について学びます。
コミュニティ
OpenTextのコミュニティをご利用ください。 個人や企業とつながり、インサイトやサポートを得ることができます。 ディスカッションに参加する。
-
顧客、パートナー、従業員がOpenText Documentum CMについて安全に学び、共有し、質問を送信できるように設計されたプライベートグループ
OpenText Documentum CM LinkedInユーザーグループ
プレミアムサポート
複雑なIT環境に対応したミッションクリティカルなサポートを提供する専任の専門家が、OpenTextのソリューションの価値を最適化します。
-
技術および戦略的専門家による1対1の個別支援
プレミアムサポート
資格
エンタープライズコンテンツ管理ソフトウェアがグローバルコンプライアンス基準を満たしていることを確認し、規制環境におけるデータの保護、記録の管理、コンテンツの保護を実現します。
OpenText Documentum Content Management for Life Sciences resources

Managing quality and manufacturing documentation for life sciences
Watch the video
Get rid of costly dead-weight data with information archiving solutions
Watch the video-
OpenText Documentum CM for Life Sciences helps manage documents by keeping them organized and compliant with rules. It speeds up clinical trials, regulatory submissions, and quality control with secure, easy-to-use tools.
-
OpenText Documentum CM for Life Sciences organizes trial documents, checks for errors like missing approvals, and lets teams share files securely. This cuts delays and keeps everything ready for inspections.
-
OpenText Documentum CM for Life Sciences uses templates and workflows to create submission-ready documents fast, helping organization meet FDA and EMA rules with clear audit trails.
-
It manages GMP documents with templates to reduce errors, simplify reviews, and ensure secure, traceable printing for compliance.
-
Yes, it connects with existing systems like CTMS, QMS, LMS, and LIMS. That means your data flows smoothly between systems, and you don’t have to switch back and forth.
-
It lets you securely print controlled copies with watermarks, expiration dates, and access logs, helping meet GxP and audit requirements.
-
No, you can run it on-premises, in your own private cloud, or with a public cloud provider. It’s flexible, so you can choose what works best for your team.

What’s new in OpenText Documentum for Life Sciences solutions
Learn about the latest new functionality and how it can benefit your organization.
Read the blog
What’s new in OpenText Documentum Content Management
Learn about the latest new functionality and how it can benefit your organization.
Read the blog










